Energie gilt als schwieriges Thema. In der Physik wird sie häufig ganz abstrakt nur als Bilanzierungsgröße betrachtet. Energie zu bilanzieren ist praktisch, da man verschiedene Prozesse miteinander vergleichen kann. Das ist beispielsweise ökologisch bedeutsam, um die Produktivität und Effizienz in Nahrungsketten und Ökosystemen zu berechnen.
Energie als Bilanzierungsgröße zu verwenden ist sinnvoll, erfordert jedoch ein großes Abstraktionsvermögen. Wie soll man sich etwas vorstellen, das man nur als Bilanz, das heißt als Mengenangabe kennt? Wenn dann beispielsweise von „Energiefluss“ die Rede ist, muss sich jeder Lernende (und Lehrende) fragen: „Was fließt denn da?“ Um Energie zu verstehen, muss man über Mengenangaben hinausgehen. Sie wird daher selbst in wissenschaftlichen Darstellungen meist recht anschaulich umschrieben. Für ein zutreffendes Verständnis müssen die Umschreibungen jedoch fachlich geklärt werden.
Energieumwandlung?
Ein bekannter Ökologe formuliert, dass Sonnenenergie bei der Photosynthese in Glukose umgewandelt werde. Energie wird jedoch nicht umgewandelt, schon gar nicht in einen Stoff. Energie ist Energie, bleibt unverändert und wird nichts Anderes. Es sei denn beim Urknall.
Energieformen?
Man redet von chemischer Energie und Bewegungsenergie, gar von Windenergie und Atomenergie. Auch hier gilt: Energie ist Energie und nichts Anderes. Daher gibt es streng genommen keine verschiedenen Energieformen: Unterschiedlich ist nicht die Energie, sondern die Formen, in denen Energie gespeichert oder übertragen wird. Beispielsweise spricht man besser nicht von chemischer Energie, sondern von chemisch gespeicherter bzw. chemisch übertragener Energie. Damit wird klar: Energie verändert sich bei Speicherung und Übertragung nicht! Sie bleibt Energie, nur die Speicherung oder die Übertragung sind unterschiedlich.
Energiereiche Stoffe?
Die Ausdrucksweise, dass Nährstoffe, Treibstoffe oder ATP (Adenosintriphosphat) „energiereich“ seien, nährt die Alltagsvorstellung, dass Energie eine stoffähnliche Substanz sei, die in den Stoffen enthalten ist. In ihnen steckt jedoch niemals Energie. Nicht Stoffe liefern Energie, sondern exergone chemische Reaktionen. Entsprechend werden Nährstoffe vom Organismus nicht durch Abbau energetisch genutzt, sondern durch Umsetzen mit Sauerstoff. Um Nährstoffe energetisch zu nutzen, müssen wir also nicht nur essen, sondern auch atmen! Der Zusammenhang von Ernährung und Atmung ist leider nur selten bewusst und wird im Unterricht meist ungenügend behandelt. Im Prozess der Zellatmung werden (abgebaute) Nährstoffe mit Sauerstoff umgesetzt. Beim Prozess der Zellatmung kommen also die mit Atmung und Ernährung aufgenommenen Stoffe zusammen, weshalb er ebenso gut „Zellernährung“ heißen könnte.
Energieträger?
Kein einzelner Stoff kann allein chemische Energie bereitstellen, sondern nur bestimmte chemische Systeme. Energieträger sind also nicht Nährstoffe, Treibstoffe oder Kohle, sondern chemische Systeme: Nährstoffe Sauerstoff, Treibstoffe- Sauerstoff, Kohle-Sauerstoff. Weil Sauerstoff allgegenwärtig ist, vergessen wir seine Rolle gern und setzen sie einfach voraus. Man beachte aber: Bei Kalorienangaben von Nahrungsmitteln handelt es sich um ihren Brennwert (Name!).
Energiereiche Bindungen?
Das Fachwort „Bindungsenergie“ suggeriert, dass Energie in chemischen Bindungen steckt. Die sogenannte Bindungsenergie bezeichnet jedoch die Energiemenge, die aufgewendet werden muss, um die Bindung zu spalten. Spalten von Bindungen erfordert Energie, Herstellen von Bindungen liefert Energie, und zwar umso mehr, je stärker die entstehenden Bindungen sind. Bei einer exergonen Reaktion haben daher die Produkte in der Summe stärkere Bindungen als die Reaktanden. Im Fall der Knallgasreaktion sind die Bindungen im Wassermolekül stärker als die in den Wasserstoff- und Sauerstoffmolekülen – siehe Abbildung 1.

Es gibt also keine energiereichen Bindungen, sondern nur schwache Bindungen. Chemische Systeme mit schwachen Bindungen sind energetisch nutzbar. Dieser Zusammenhang kann anhand der Prozesse von Photosynthese und Zellatmung verdeutlicht werden. Chemisch sind beide Prozesse gegenläufig, die Summenformeln lauten:

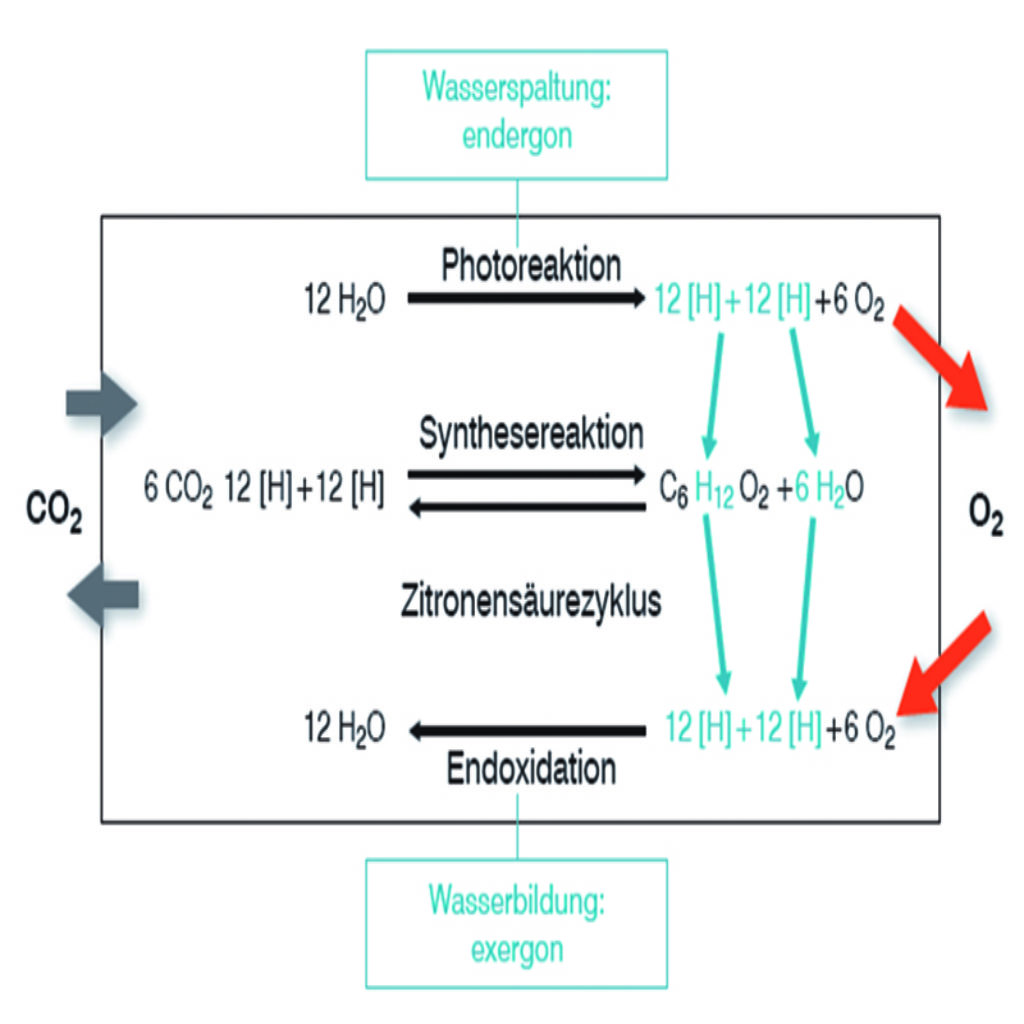
Auch die Teilprozesse können parallelisiert werden, wobei die endergone Wasserspaltung (durch Nutzung der Energie des Lichts, Photoreaktion der Photosynthese) und die exergone Wasserbildung (Endoxidation der Zellatmung) sowie Synthese Reaktion der Photosynthese (Calvinzyklus) und Zitronensäurezyklus der Zellatmung aufeinander bezogen werden. Der Weg der Wasserstoffatome von der Wasserspaltung bis zur Wasserbildung – blau gekennzeichnet – kann in Abbildung 2 anschaulich nachvollzogen werden.
Dr. Ulrich Kattmann, Professor für Didaktik der Biologie an der Universität Oldenburg (i. R.) . Über 45 Jahre Vermittlung von Themen zur
Biologie, vor allem Evolution und Genetik, in Universität, Schulen, zahlreichen Vorträgen, Aufsätzen und Büchern.
Zum Weiterlesen: Der hier vorliegende Beitrag basiert auf dem Buch von Ulrich Kattmann: Neue Wege in die Biologie – Energienutzung durch Organismen. Buch für Lernende des Sekundarbereichs II. Seelze: Friedrich Verlag 2019. Zu Energiebilanzen vgl.: Mathias Trauschke (2016). Energie fließend verstehen, MINT Zirkel 3-2016












